Kurzerklärung
Zunächst eine kurze Erläuterung zum Fragilen-X Syndrom (kurz FraX), eine ausführliche Erläuterung findet sich weiter unten beginnend bei “Chromosomen”.
Ursache des FraX ist ein vererbter genetischer Defekt. Zunächst beginnt sich dieser Gendefekt unbemerkt von Generation zu Generation in mehreren Stufen über die sogenannte Prämutation zu entwickeln, bis er schließlich in Form der Vollmutation zur Folge hat, dass das betreffende Gen nicht mehr funktioniert. Dadurch wird ein für die Entwicklung vor allem der Gehirnzellen und ihrer Verbindungen untereinander wesentlicher Baustein (ein “Protein“) nicht mehr gebildet und es kommt zur Ausprägung des Fragilen-X Syndroms.
Chromosomen
Das Erbgut des Menschen ist in 46 Chromosomen unterteilt, 23 davon stammen von der Mutter und 23 vom Vater. Paarweise dargestellt sieht dies so aus:
Abbildung der 23 Chromosomenpaare eines Mannes (Abbildung mit freundlicher Genehmigung des Zentrums für Humangenetik, Uni Bremen).
Das 23. Paar bestimmt das Geschlecht eines Menschen. Frauen haben je ein X-Chromosom von der Mutter und vom Vater. Männer besitzen ein X-Chromosom von der Mutter und ein Y-Chromosom vom Vater.
Gene
CGG-Wiederholungen
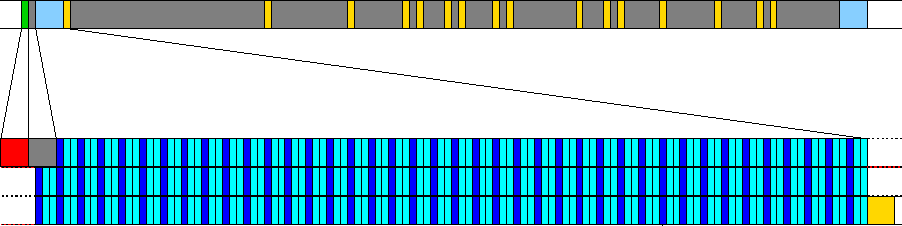
In diesem Fall wird das Gen durch Anlagerung von Methylgruppen im Promotor abgeschaltet, eine Produktion von FMRP findet nicht mehr statt und es kommt zur Ausprägung des Fragilen-X Syndroms.
Der genaue Erbgang des FraX wird ->hier beschrieben.
Bemerkung: Es gibt seltene Fälle, in denen der Ausfall des FMR1-Gens durch eine sogenannte “Deletion” hervorgerufen wird. Dabei handelt es sich um das Fehlen eines Abschnitts auf dem Gen, also nicht die Verlängerung der CGG-Sequenz, die zur Dysfunktion des Gens führt.
Auswirkungen des FMR1-Protein-Mangels
Heute weiß man, dass das FMR1-Protein (=FMRP), das bei FraX-Kindern ausfällt, am Stoffwechsel von chemischen Botenstoffen (Neurotransmittern) in den Dendriten der Gehirnzellen beteiligt ist. Das Fehlen von FMRP führt zu einer dauerhaften Übererregung der Synapsen und schließlich zur Degenerierung der Dendriten. Dadurch gehen wichtige neuronale Verbindungen dauerhaft verloren.
FMRP reguliert den durch die Neurotransmitter ausgelösten Stoffwechsel. Es bindet sogenannte mRNA (ein Zwischenprodukt bei der Proteinsynthese) verschiedener Proteine und wirkt dabei zudem selbstregulierend. Der genaue Stoffwechsel ist noch nicht erforscht, allerdings beschäftigen sich damit zur Zeit weltweit verschiedene Forschergruppen. In den vergangenen Jahren gab es zunehmend Versuche, auf verschiedene Weisen in den beim Fehlen von FMRP veränderten Stoffwechsel regulierend einzugreifen, um letztendlich zu einer gezielten medikamentösen Therapie von Fragilem-X zu gelangen.
Fragen und Antworten
Was ist ein "Mosaik"?
Ein Mosaik (ganz allgemein) bedeutet, dass nicht in allen Körperzellen der gleiche genetische Zustand herrscht, z.B. bei Frax ein Teil der Zellen “nur” eine Prämutation aufweist, der andere Teil aber schon in eine Vollmutation übergegangen ist. Dies kann passieren, wenn die Mutter schon eine relativ hohe Prämutation hat, aber eben gerade noch nicht so hoch, dass in jeder Zelle daraus eine Vollmutation wird. Diese “gemischt” betroffenen Kinder können dadurch leichter betroffen sein, als die “komplett” Vollmutierten.
Durch eine Methylierung (ganz allgemein) schaltet eine Zelle bestimmte Genabschnitte “stumm”. Zellen machen das auch, um Genabschnitte, in denen irgendwas “faul” ist – vorsichtshalber – zu inaktivieren (damit z.B. nicht ein falsches Eiweiß gebildet wird). Beim Frax (Vollmutation) passiert dieses auch. Die Zelle merkt, wenn die kritische Grenze von ca. 200 CGG Tripletts überschritten ist, dass hier etwas nicht stimmt und methyliert diesen Bereich, wodurch er ausgeschaltet wird. Der Genabschnitt kann nicht mehr abgelesen werden, dadurch wird im Verlauf das FMR-Protein nicht mehr hergestellt. Sein Fehlen bedingt die Behinderung der betroffenen Kinder. Beim Frax ist noch interessant, dass “nur” der Starterbereich des eigentlichen Gens kaputt ist, gar nicht der eigentlich wichtige Genabschnitt, an dem das FMR-Protein abgelesen wird (die Lampe, die Licht machen soll ist in Ordnung, nur der Schalter, der sie anmacht, ist kaputt).
Bei dieser Methylierung kann es nun auch zu einem Mosaik kommen, d.h. nicht in jeder Zelle wird der “defekte” Genabschnitt “stummgeschaltet”. Insbesondere nahe an der “kritischen Grenze” kann das passieren, so dass nur in einem Teil der Zellen kein FMR-Protein gebildet wird. Der andere Teil hat zwar auch hohe Triplettzahlen, aber bildet trotzdem noch das FMR-Protein, so dass auch hier die Beeintächtigung durch den Gendefekt deutlich leichter ausfallen kann.
Prof. Steinbach (Genetiker) sagte vor Jahren, erst ab einer Höhe von mindestens 40 % nicht betroffener (also nur prämutierter) Zellen könne man laut Fachliteratur davon ausgehen, dass die kognitiven Fähigkeiten besser seien als die anderer Jungs / Männer mit Vollmutation.
Fazit:
- Man muss unterscheiden zwischen einem (weniger bedeutenden) Expansions-Mosaik, das wohl häufiger vorkommt, und einem (vermutlich positiver zu bewertenden) Methylierungsmosaik, das es jedoch seltener gibt.
Expansions-Mosaik heißt: In einem Teil der Zellen liegt eine Vollmutation vor, in einem anderen Teil nur eine Prämutation.
Methylierungs-Mosaik heißt: Ein Teil der vollmutierten Zellen ist unmethyliert (= nicht stumm geschaltet), ein anderer Teil methyliert.
- In der wissenschaftlichen Literatur ist man sich absolut uneinig in der Frage, ob überhaupt und in welchem Maße sich Mosaikbefunde auf die kognitve Entwicklung betroffener Kinder (positiv) auswirken.
– In einer Studie (Warren) stellte sich heraus, dass Männer ohne Mosaikbefund (in ihren Blutzellen) gleichwohl in ihren Gehirnen, die nach ihrem Tod untersucht wurden, neben den vollmutierten auch prämutierte Zellen aufwiesen, was die Vermutung nahelege, alle Männer mit Fragilem-X-Syndrom hätten eine Art Mosaikbefund – zumindest im Gehirn.
– Unter folgendem Link ist nachzulesen, dass nach Warrens Auffassung ein Mosaikbefund vermutlich keine positive Auswirkung für die betroffenen Menschen hat: “For a long time we thought mosaic patients would be less severely affected,” Warren said. “But in fact, they are usually just as affected as classic fragile X patients whose gene is turned off.’ ” Sinngemäße Übersetzung: “Lange dachte man, Mosaik-Patienten seien weniger betroffen. Aber in Wirklichkeit sind sie gewöhnlich ebenso betroffen wie klassische Patienten mit Fragilem-X-Syndrom…”
http://www.emory.edu/EMORY_REPORT/erarchive/1995/June/ERjune.5/6.5.95warren’s.res.html
– Bei Hagerman (Fragile X – Treatment and developement) ist zu lesen, dass ein Expansions-Mosaik (je nach Anzahl der prämutierten Zellen) eine leichte Verbesserung der kognitiven Fähigkeiten bedeutet (IQ 60 +/- 15), (im Vergleich dazu bei “normaler” Vollmutation IQ 50), dass aber ein Methylierungs-Mosaik sehr wohl eine deutlich günstigere Prognose bedeute – mit einem durchschnittlichen IQ von 88 – also im unteren Normbereich.
Ganz selten kommt ein Methylierungsdefekt, d.h. ein zusätzlicher zweiter Gendefekt, bei Frax vor: das ist in der Literatur bei Fraxmännern mit Vollmuation beschrieben, die ganz “normal” sind. Da wird trotz Vollmutation der defekte Genabschnitt einfach nicht abgeschaltet. Sie bilden ganz normal das FMR-Protein, denn der Starterbereich wird nicht inaktiviert, das Gen wird normal abgelesen.
Bei vollmutierten Frauen liegt – quasi natürlicherweise (wie bei jeder gesunden Frau) – immer eine Mosaikkonstellation vor, da immer eines der beiden X-Chromosomen in der jeder Zelle „stumm geschaltet“ wird. So kann bei betroffenen Frauen im Gehirn (nach Zufallsprinzip verteilt) überwiegend das X-Chromosom mit dem Fraxallel „stumm geschaltet“ und ihr zweites, gesundes X aktiv sein. Diese Frauen sind dann u.U. nur sehr wenig oder auch gar nicht von Fraxsymptomen betroffen. Liegt jedoch der umgekehrte Fall vor, so dass überwiegend das Frax-Gen im Gehirn aktiv ist, können die Frauen ähnlich schwer beeinträchtigt sein wie Männer mit Vollmutation.